
【药品名称】
通用名称:西他沙星片
英文名称:Sitafloxacin Tablets
汉语拼音:Xitashaxing Pian
【成份】
活性成分:西他沙星
化学名称:(-)-7-[(7S)-7-氨基-5-氮杂螺[2.4]-5-庚基]-8-氯-6-氟-1-[(1R,2S)-2-氟环丙基]-1,4-二氢-4-氧代-喹啉-3-羧酸倍半水合物
化学结构式:
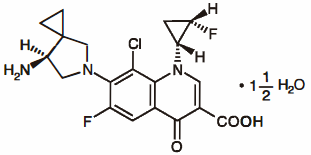
分子式:C19H18ClF2N3O3·11/2H2O
【性状】
本品为白色至微黄色薄膜衣片,除去包衣后显微黄色至淡黄色。
【适应症】
适用于对本品敏感的金黄色葡萄球菌、凝固酶阴性葡萄球菌等葡萄球菌属;肺炎链球菌、化脓性链球菌、无乳链球菌等链球菌属;粪肠球菌、屎肠球菌等肠球菌属;卡他莫拉菌;大肠埃希菌;柠檬酸杆菌;肺炎克雷伯菌等克雷伯菌属;产气肠杆菌、阴沟肠杆菌等肠杆菌属;粘质沙雷菌等沙雷菌属;奇异变形杆菌等变形杆菌属;摩根摩根菌;流感嗜血杆菌;铜绿假单胞菌;消化链球菌等消化链球菌属;普雷沃菌;牙龈吓啉单胞菌等吓啉单胞菌属;梭杆菌属;沙眼衣原;肺炎支原体;肺炎衣原体;嗜肺军团菌所引起的下列感染;
О咽炎、喉炎、扁桃体炎(包括扁桃体周炎、扁桃体周脓肿)、急性支气管炎、感染性肺炎、慢性呼吸系统疾病的继发感染
О膀胱炎、肾盂肾炎、尿道炎
О宫颈炎
O中耳炎、鼻窦炎
O牙周炎、冠周炎、颌骨骨炎
【规格】
50 mg(按C19H18CIF2N3O3计)
【用法用量】
口服,成人一次50mg (1片),一日2次;或一次100mg (2片),一日1次;疗效不理想的患者可一次100mg (2片),一日2次。
【不良反应】
在日本的临床试验中,总病例1,220例中有409例( 33.5%)出现不良反应(包括实验室检查值异常)。主要的不良反应为:腹泻69例(5.7%)、松软便86例(7.0%)、头痛26例(2.1%)、ALT (GPT)升高72例(5.9%)、AST ( GOT)升高59例(4.8%)、嗜酸粒细胞计数增多47例(3.9%)等。
在上市后临床试验中(时间:2008年12月~2010年11月,日本),总病例3,331例中有148例(4.4%)出现不良反应(包括实验室检查值异常)。主要的不良反应为:腹泻41例(1.2%)、松软便14例(0.4%)、ALT (GPT)升高22例(0.7%)、AST ( GOT)升高16例(0.5%)、皮疹12例(0.4%)等。
(1)临床重大不良反应
1)休克、速发过敏反应(发生率不明[注]):可能会出现休克或速发过敏反应,因此应密切观察。如发现血压下降、呼吸困难、皮疹、血管性水肿等异常时,停止给药并采取适当的处理措施。
2)眼粘膜皮肤综合征(史蒂文斯-约翰逊综合征)(发生率不明[注]):可能发生眼粘膜皮肤综合征,故应密切观察,遇有异常应停止给药并采取适当的处理措施。
3)急性肾损伤(发生率不明[注]):曾有急性肾损伤的报道,故应密切观察,遇有异常应停止给药并采取适当的处理措施。
4)肝功能疾病(发生率<0.1%):曾有肝功能疾病包括AST(GOT)升高、ALT(GPT)升高等的报道,故应密切观察,遇有异常应停止给药并采取适当的处理措施。
5)血小板减少症(发生率不明[注]):曾有报道使用本品后出现血小板减少症,故应密切观察,遇有异常应停止给药并采取适当的处理措施。
6)假膜性结肠炎(发生率不明[注]):可能会发生假膜性结肠炎。如出现腹痛、频繁腹泻,应停止给药并采取适当的处理措施。
7)低血糖症(发生率<0.1%):有报道出现低血糖症,甚至出现低血糖昏迷,故应密切观察。遇有异常应停止给药并采取适当的处理措施。低血糖症多出现在糖尿病患者、肾功能损害和老年人群。
8)意识模糊、儋妄、幻觉等精神系统症状(发生率不明[注]):曾有报道使用本品后出现意识模糊、儋妄、幻觉等精神系统症状。故应密切观察,遇有异常应停止给药并采取适当的处理措施。
(2)其他的喹诺酮类抗菌药临床重大不良反应
其他的喹诺酮类抗菌药曾报告过以下临床重大不良反应。故使用本品时亦应密切观察,出现以下异常应停止给药并采取适当的处理措施。
1)中毒性表皮坏死松解症(TEN) ;
2)惊厥;
3)QT间期延长、室性心动过速(包括尖端扭转性室性心动过速);
4)黄疸;
5)间质性肺炎;
6)横纹肌溶解;
7)肌腱病变;
8)粒细胞缺乏症;
9)全血细胞减少症;
10)溶血性贫血;
11)重症肌无力加重。
(3)其他不良反应
可能会出现下述不良反应,当出现异常时应采取适当的处理措施,必要时停药。
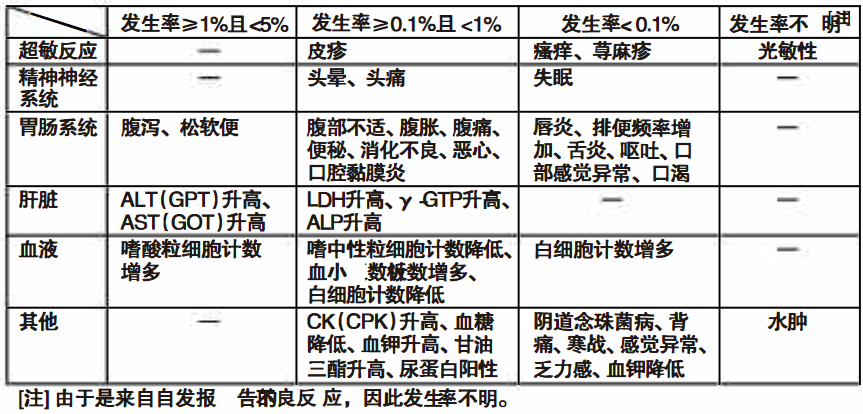
【禁忌】
以下患者禁用本品:
1.对本品的成分或其他喹诺酮类抗菌药有过敏史的患者;
2.妊娠期或可能妊娠的妇女(参考【孕妇及哺乳期妇女用药】);3.儿童(参考【儿童用药】)。
【注意事项】
1.慎重给药(以下患者应慎重给药)
(1)肾功能损害患者[持续升高血药浓度(参考【药代动力学】);
(2)患有癫痫等惊厥性疾病或有相关既往史的患者(同类药物有诱发惊厥的报告);
(3)重症肌无力患者(同类药物有重症肌无力加重的报告);
(4)老年人(参考【老年用药】)。
2.用法用量相关的注意事项
(1)使用本品时为防止出现耐药菌等,原则上应确认细菌敏感性,将用药时间控制在疾病治疗所需的最短时间内。
(2)肾功能损害患者用药后血药浓度会升高,故须调整给药剂量和给药间隔(参考【药代动力学】)。
3. 治疗作用相关的使用注意事项
本品引发腹泻、松软便的发生率相对较高,故使用时须充分考虑风险获益的平衡(参考【不良反应】)。
在治疗咽炎、喉炎、扁桃体炎(包括扁桃体周炎、扁桃体周脓肿)、急性支气管炎、鼻窦炎时,需要参考相关的抗生素合理用药指南。在判断适合使用该药时,才使用该药。
4. 其他注意事项
本品为PTP包装,请指导患者将药品从PTP板中取出后服用(有报道因误服PTP板后导致食管粘膜损伤,以及PTP板尖锐的边角引起穿孔,诱发纵隔炎等严重并发症)。
【孕妇及哺乳期妇女用药】
1. 妊娠期或可能妊娠的妇女禁用本品(尚未确立妊娠期间用药的安全性)。
2. 哺乳期妇女用药期间应停止哺乳[动物实验结果显示本品可经大鼠的乳汁分泌]。
【儿童用药】
尚未确立本品对出生时低体重儿、新生儿、婴儿、幼儿和儿童的用药安全性。在动物实验中观察到幼犬关节软骨损伤;来自中国仓鼠的培养细胞,经过光照射后,发现可诱发染色体异常。故对上述人群禁用本品。
【老年用药】
—般老年人的生理功能均有所降低,故应密切观察患者的状态,慎重给药(参考【药代动力学】)。
【药物相互作用】
本品与下列药物合并用药时应注意: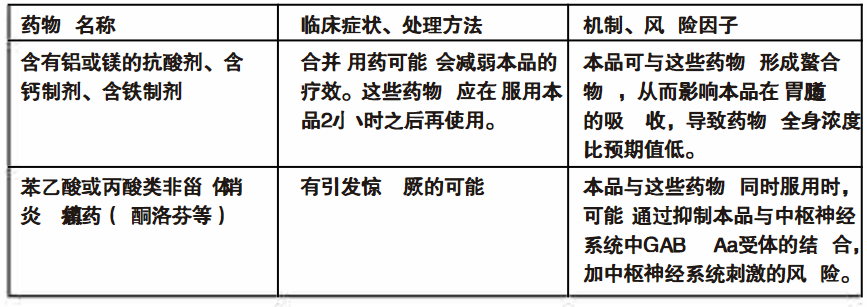
【药物过量】
一日1次或2次口服本品500mg后,经紫外光照射出现光毒性。
另外,一日2次静脉注射本品400~800mg,出现剂量依赖性的QT间期延长,平均变化幅度在10msec或以下。
【临床试验】
1.各类疾病的有效率
在以呼吸道感染、尿路感染、耳鼻喉感染、牙齿感染、口腔手术区域感染及生殖器官感染患者为研究对象的临床试验中,给予患者西他沙星50mg一日2次或100mg一日1次或2次,各疾病的有效率如下表:
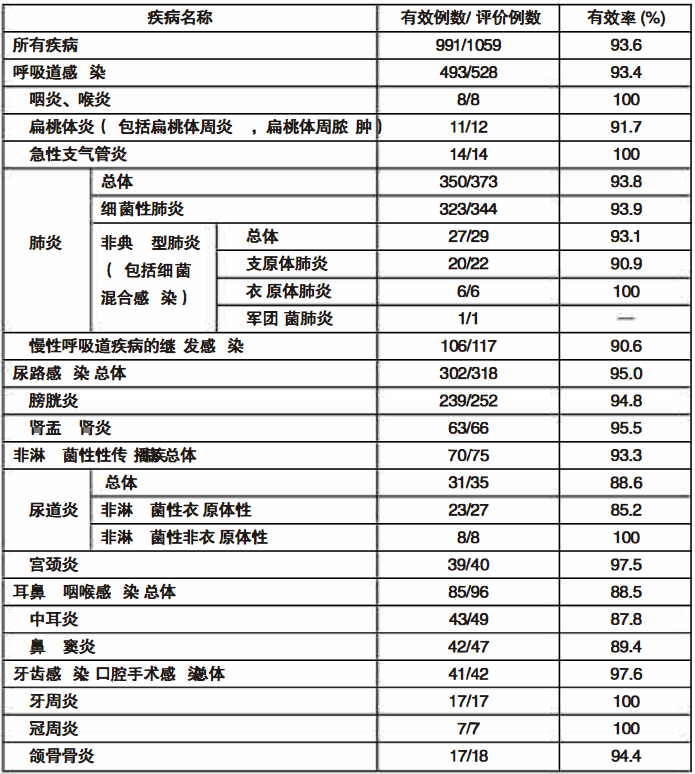
2. 对病原微生物的清除率
以呼吸道感染、尿路感染、耳鼻喉感染、牙齿感染、口腔手术区域感染及生殖器官感染患者为研究对象,根据临床试验收集的病原微生物的清除率见下表:
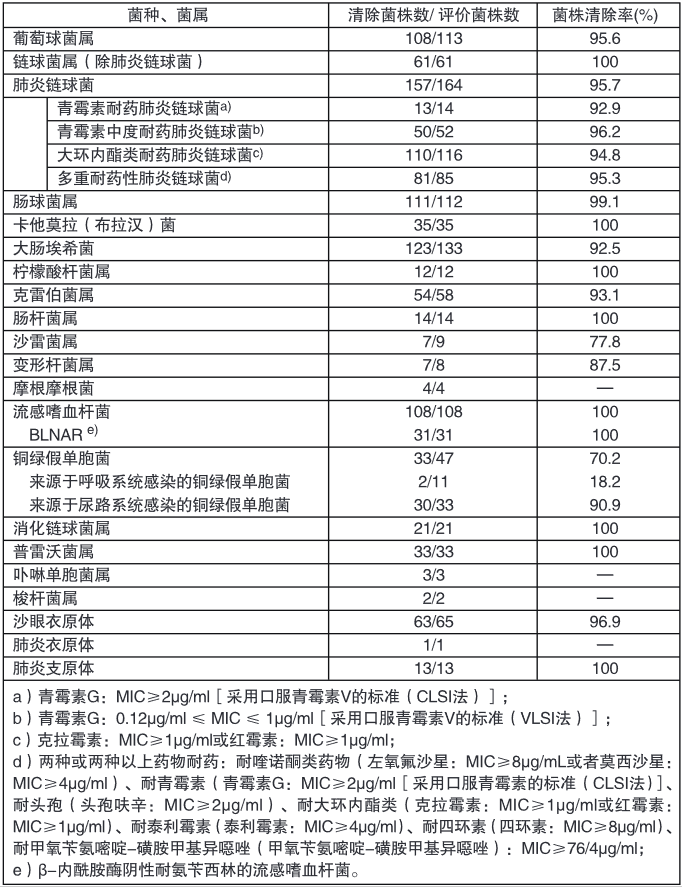
【药理毒理】
药理作用
西他沙星为喹诺酮类抗菌药,通过抑制细菌DNA旋转酶和拓扑异构酶IV的活性发挥杀菌作用。西他沙星对需氧和厌氧的革兰阳性菌和革兰阴性菌、非典型病原体都有广谱抗菌作用,对葡萄球菌属、链球菌属、肺炎链球菌、肠球菌属、卡他莫拉菌、大肠埃希菌、柠檬酸杆菌属、克雷伯菌属、肠杆菌属、沙雷菌属、变形杆菌属、摩氏摩根菌、流感嗜血杆菌、铜绿假单胞菌、嗜肺军团菌、消化链球菌属、普雷沃尔菌属、吓啉菌属、梭形杆菌属、沙眼衣原体、肺炎衣原体、肺炎支原体等有抗菌作用。
在以呼吸系统感染患者为受试者的临床试验中进行了PK/PD分析,结果显示病原菌的清除率随着AUC0-24hrMIlC或CmaxMIlC的升高而增加。AUC0-24hr/MIC超过100时,有22株肺炎链球菌在内的呼吸系统感染的主要病原菌的清除率达96.3% (78/81),Cmax/MlC超过5时达96.3% ( 79/82)。此外,以肺炎球菌性呼吸道感染患者为受试者的临床试验结果显示,以西他沙星非结合形式的血药浓度计算,AUC0-24hr/MIC大于30时以及Cmax/MIC大于2时病原菌清除率均达到98.9% ( 89/90 )。
毒理研究
重复给药毒性
大鼠连续4周和连续13周经口给药的毒性试验中,尿中药物结晶(未伴发肾脏病变)和自发的骨及软骨病变加重。大鼠连续4周经口给药的毒性试验中雌雄动物的无毒性反应剂量均为46.9mg/kg/日,13周试验中均为20mg/kg/日。
食蟹猴连续4周和连续52周经口给药的毒性试验中,睾丸生精小管中精细胞数量减少,血清磷脂有轻度增加。食蟹猴连续4周经口给药的毒性试验中雌雄动物的无毒性反应剂量均为28.1mg/kg/日,52周试验中均为25mg/kg/日。
遗传毒性
西他沙星Ames试验、体外染色体畸变试验及小鼠淋巴瘤TK试验结果均为阳性,体内微核试验、程序外DNA合成试验及显性致死试验均为阴性。
生殖毒性
西他沙星对大鼠亲代动物未见生殖毒性,但家兔试验中出现了一般抗菌药物常见的流产动物数增加的现象。西他沙星对胚胎和胎仔有轻度影响,但对大鼠和家兔未见致畸作用。
关节毒性
西他沙星在幼犬中引起关节软骨空洞、糜烂,但在成年犬中未见关节毒性。光毒性
小鼠光毒性试验中,白化小鼠及有色小鼠的无毒性反应剂量分别为20mg/kg及93.8mg/kg。
光遗传毒性
光照下的体外染色体畸变试验结果为阳性,但光照下的体内小鼠试验中,20mg/kg剂量下试验结果为阴性。
【药代动力学】
1. 血清药物浓度
健康成人在空腹及餐后单次口服西他沙星,血清中浓度的变化及药代动力学参数如下所示。
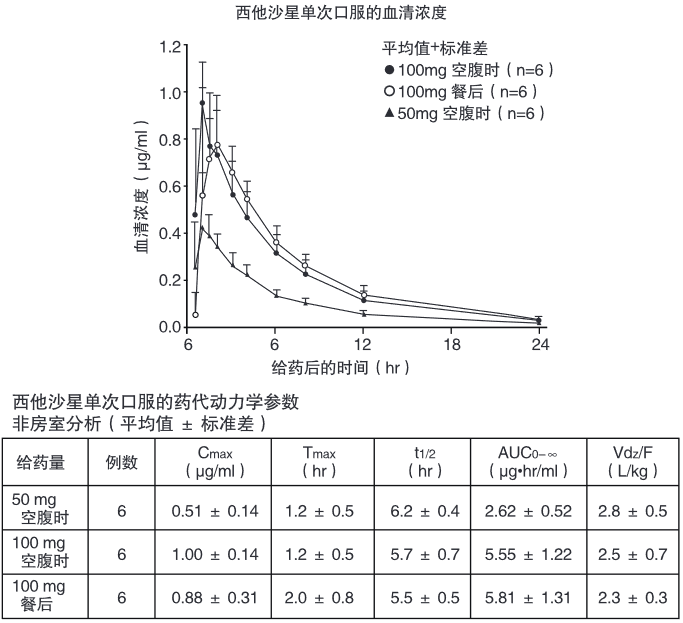
2. 血清蛋白结合率
健康成人单次口服西他沙星100mg,服药1小时、4小时、8小时后,本品与血清蛋白的结合率为46%~55%(超滤法),各时间点结合率基本恒定。
3. 分布
单次口服西他沙星50mg或100mg后,各组织及体液中浓度的变化如下所示,显示良好的组织/体液分布。
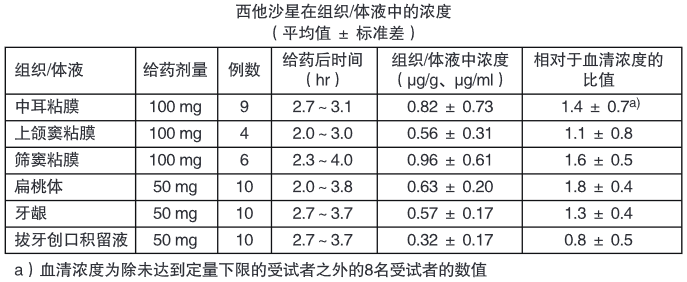
4. 代谢
西他沙星在体内大部分直接以原型药物从尿中排出,并已确认在血清、尿、粪便中可检出少量代谢物,如葡萄糖苷酸、7’-氧代物、7'S-氢氧化物、7'S-氢氧化物的葡糖苷酸、N-乙酰结合物。
采用生物样本进行的体外试验中,西他沙星对细胞色素P450中的CYP1A1和CYP1A2有较弱的抑制作用,但不会抑制CYP2C9、CYP2D6和CYP3A4等。
5. 排泄
健康成人单次空腹口服西他沙星50 mg或100 mg,给药后48小时内约70%的给药量以原型药物从尿中排出。
另外,研究显示口服碳十四标记的西他沙星100 mg后,72小时内约80%的给药量从尿中、约20%的给药量从粪便中排出。
6.肾功能损害患者的药代动力学
根据肌酐清除率(Ccr )数值将受试者分为3组,单次空腹口服西他沙星50mg,结果显示随着肾功能的降低,血清中药物浓度的消除和尿排泄均延长。
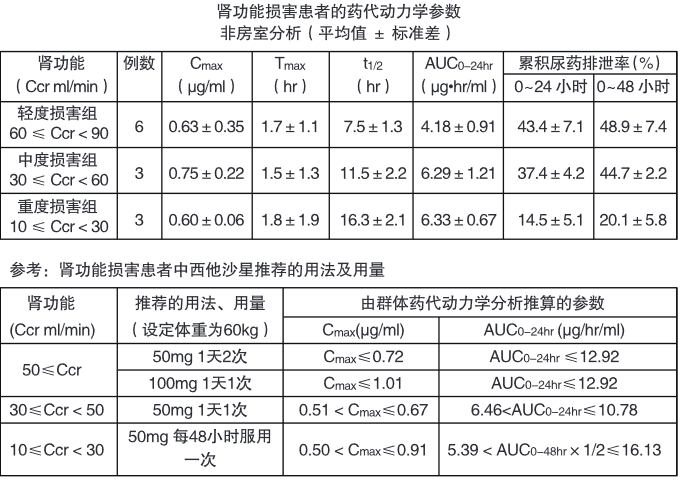
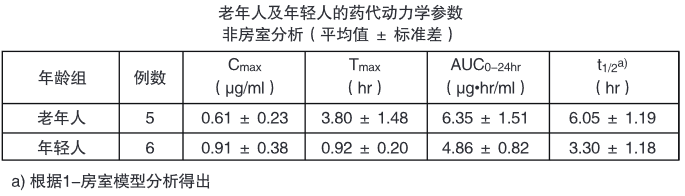
7.老年人的药代动力学
5名老年人(67~80岁)及6名年轻人(25~35岁)单次空腹口服西他沙星100mg。与年轻人比较,老年人的t1/2延长、Cmax下降及AUC0-24hr增加。结果表明随年龄增加、吸收排泄功能的下降会影响西他沙星的药代动力学。
【贮藏】
25℃以下密闭保存。
【包装】
铝塑包装,6片/盒,10片/盒,12片/盒。【有效期】
36个月。
【执行标准】
进口药品注册标准JX20110267
【进口药品注册证号】
进口药品注册证号:H20190022
【生产企业】
企业名称:DAllCHI SANKYO CO.,LTD.
地址:3-5-1,Nihonbashi Honcho, Chuo-ku,Tokyo,Japan
生产厂名称:CMIC CMO Co.,Ltd.Shizuoka Plant
生产地址:1-588, Kanaya-azuma, Shimada, Shizuoka, Japan
【国内联系单位】
企业名称:第一三共(中国)投资有限公司)
地址:中国(上海)自由贸易试验区居里路500号3幢
邮编:201203
热线:400 656 3228(工作时间:周一至周五9:00-12:00;13:00-17:30)
传真号码:021-60397396
网址: http://www.daiichisankyo.com.cn

声明:关于产品的详细处方资料请以国家食品药品监督管理局最新核准的版本为准。本网站上的产品信息非药品广告,仅作为产品知识供医学、药业专业人士参考使用。本网站上的产品信息不得取代医生或其他有资质的医疗专业人士提供的医疗建议和医疗咨询,不得用于疾病的诊断。